מחקר שנערך באוניברסיטת בן-גוריון בנגב מתקרב בכמה צעדים בודדים לרתימת תאי Tשל המטופל עצמו למאבק בסרטן. טיפול זה כרוך בבידוד של תאי T מהדם של המטופל ותכנותם מחדש במטרה לזהות ולהשמיד טוב יותר תאים סרטניים. הטיפול החדשני מבוסס על ייצור ננו-מבנים המדמים את התאים שמפעילים תאי T ומבוססים על טכנולוגיית ייצור שבבים
מחקר שנערך באוניברסיטת בן-גוריון בנגב מתקרב בכמה צעדים בודדים לרתימת תאי Tשל המטופל עצמו למאבק בסרטן. טיפול זה כרוך בבידוד של תאי T מהדם של המטופל ותכנותם מחדש במטרה לזהות ולהשמיד טוב יותר תאים סרטניים. הטיפול החדשני מבוסס על ייצור ננו-מבנים המדמים את התאים שמפעילים תאי T ומבוססים על טכנולוגיית ייצור שבבים. ממצאי המחקר פורסמו בכתב העת Advanced Materials.
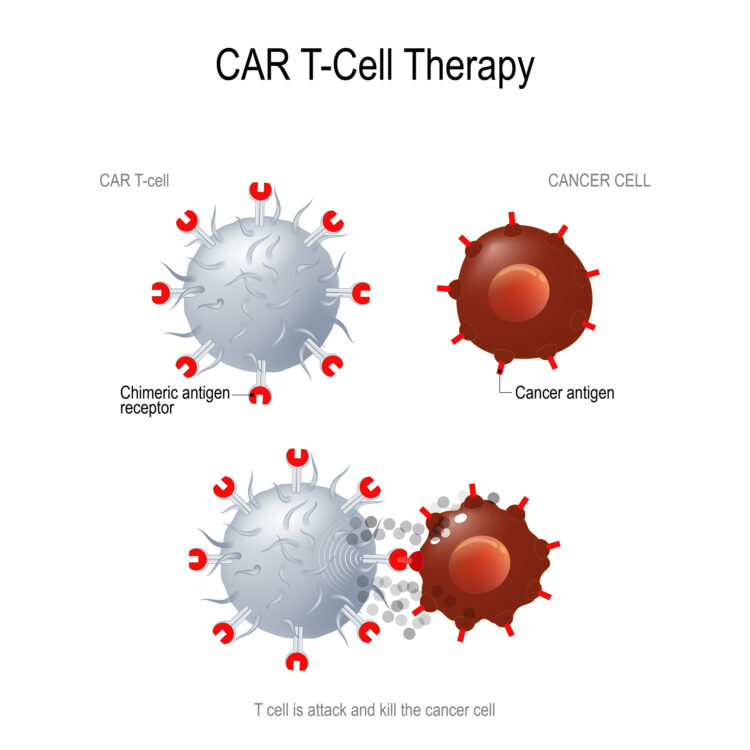
מערכת החיסון שלנו נועדה להגן עלינו על ידי זיהוי ותקיפת תאים נגועים או חולים. עם זאת, תאים סרטניים מצליחים לעתים קרובות "לרמות" את מערכת החיסון על ידי העמדת פנים שהם תאים בריאים ובכך להשבית מנגנוני תקיפה של תאי מערכת החיסון. בשנים האחרונות פותח טיפול חדשני המסייע למערכת החיסון להילחם בסרטן בצורה יעילה יותר. טיפול זה כרוך בבידוד של תאי T, שהם "החיילים הקרביים" של מערכת החיסון , מהדם של חולה, ותכנותם מחדש במעבדה כדי לזהות ולהשמיד טוב יותר תאים סרטניים.
במהלך תהליך התכנות מחדש, תאי ה- Tמופעלים באופן דומה להפעלה שלהם בגוף בעת זיהום, ומהונדסים גנטית כדי לייצר קולטנים מיוחדים על פני השטח שלהם הנקראים קולטני אנטיגן כימריים – chimeric antigen receptors (CAR) שבאמצעותם תאי T מהונדסים מזהים תאי סרטן מסוגים ספציפיים. לאחר הגדלת הכמות של התאים המתוכנתים מחדש, המכונים כיום תאיCAR T , מוזרקים אלה בחזרה לדם חולה, שם הם פועלים בדיוק מירבי, מוצאים ומשמידים תאי סרטן שמערכת החיסון הטבעית עלולה להתעלם מהם.
טיפול בתאי CAR T נחשב למהפכה בריפוי סרטן, ומציע מספר יתרונות על פני כימותרפיה מסורתית. הוא מספק מיקוד מדויק של סוגי סרטן ספציפיים, משתמש בתאי החיסון של החולה עצמו לטיפול מותאם אישית, ומוכיח הצלחה יוצאת דופן בטיפול בסוגי סרטן דם, כמו לוקמיה ולימפומה, שלעתים קרובות אינם מגיבים לטיפולים קונבנציונליים. עם זאת, למרות ההבטחה הגלומה בו, הטיפול באמצעות תאי CAR T עדיין מוגבל. אחת הסיבות המרכזיות הינה אורך הפעולה הקצר של תאיCAR T , שמותשים במהרה לאחר הזרקה לדם של המטופל.
כדי להתמודד עם בעיה זו, שתי קבוצות מחקר מאוניברסיטת בן-גוריון בנגב, בראשות פרופ' מארק שוורצמן מהמחלקה להנדסת חומרים ופרופ' אנג'ל פורגדור מהמחלקה לאימונולוגיה, שתפו פעולה במטרה לחקור מדוע תאי T נשארים פעילים בגוף במהלך תגובות חיסוניות טבעיות אך מאבדים במהירות תפקוד כאשר הם מופעלים ומהונדסים גנטית באופן מלאכותי במעבדה. הם שיערו כי הבדל עיקרי טמון במאפיינים הפיזיים של הסביבה שמפעילה את התאים: במעבדה, תאי T בדרך כלל מגורים באמצעות חרוזי פלסטיק נוקשים המצופים במולקולות מפעילות. בגוף, לעומת זאת, תאיT מגורים על ידי תאים נושאי אנטיגן, תאים לא תקינים או תאים נגועים, שהם בדרך כלל רכים ואלסטיים, עם משטחים מורכבים המכוסים בבליטות ננומטריות הדומות לזרועות זעירות.
אי לכך הם הנדסו משטחים מלאכותיים מכוסים בננו-מבנים המחקים את אלה שעל תאים המגרים תאי T בגוף. החוקרים גילו שתאי T אנושיים שנלקחו מדגימות דם והופעלו על משטחים מלאכותיים אלה, הציגו הפעלה חזקה וארוכת טווח משמעותית, המדמה את סביבתם הטבעית. יתר על כן, הם הבינו שניתן לכוונן את עוצמת הגירוי על ידי התאמת הגיאומטריה והקשיחות של הננו-מבנים, ממצאים שפרסמו במספר מאמרים בשנים האחרונות.
מעודדים מממצאים אלו, פרופ' שוורצמן ופרופ' פורגדור הציבו לעצמם את המטרה השאפתנית הבאה: לתכנן משטחים מלאכותיים בעלי ננו-מבנה המותאמים במיוחד ליצירת תאי CAR T חזקים ובעלי פעילות נגד סרטן לטווח ארוך.לשם כך, הם יצרו ספרייה של משטחים עם ננו-גיאומטריות וקשיחויות מכניות מגוונות והעריכו את השפעתם על מספר קריטריונים של הצלחה בתגובת תאי T כמו: אופן ההפעלה, תשישות, התרבות ותכנות מחדש של .CAR T
"פתאום", סיפר פרופ' פורגדור, "מצאנו את עצמנו מוצפים בנתונים מעיצובי משטחים שונים. מעבר לעובדה שנעשה שימוש בתאי T של תורמים מרובים, שלכל אחד מהם תגובות ספציפיות לאדם, זה הרגיש כמו תחרות רב- קרב, שבה כל שהיינו צריכים זה לזהות את המתחרה בעל ההישגים הטובים ביותר."
כדי לפתור את הבעיה, הם שיתפו פעולה עם עמיתם ד"ר אופיר כהן, ביואינפורמטיקאי שהשתמש בניתוח חישובי מתקדם כדי לזהות את המשטח המבטיח ביותר, על סמך מדדי ביצועים מצטברים. המשטח שנבחר סיפק הפתעות נוספות. תאי CAR T שנוצרו בעזרתו ביטאו רמות גבוהות של גנים הקשורים לפעילות אנטי-סרטנית ארוכת טווח, במיוחד אלו הקשורים לתת-אוכלוסייה המכונה "תאי T עם זיכרון מרכזי", שהם המפתח לטיפול יעיל בסרטן. ואכן, תאי CAR T שיוצרו באמצעות משטח זה הכילו משמעותית יותר מתאי זיכרון מרכזיים מאשר אלו שיוצרו באמצעות חרוזי פלסטיק קונבנציונליים. בהמשך, החוקרים הראו שתאי CAR T המופקים באמצעות המשטח עם הנו-מבנים, הם בעלי יכולת זיהוי והשמדת תאי סרטן הרבה יותר חזקה וארוכת טווח לעומת תאי T CAR המופקים בשיטות קיימות, באמצעות מספר ניסוים במעבדה ובמודלים של עכברים. כעת, מתמקדים החוקרים בהרחבת הטכנולוגיה שלהם ובמעבר ממעבדת המחקר ליישום קליני.
"כדי לייצר ננו-מבנים מפעילים אלה השתמשנו בתחילה בטכניקות שהותאמו מטכנולוגיית ייצור שבבים", הסביר פרופ' שוורצמן. "הביקוש המתמשך לרכיבים אלקטרוניים קטנים יותר ויותר בשבבים הביא את הטכנולוגיה הזו לנקודה שבה ניתן לייצר מבנים כמעט בכל גודל, אפילו ברמה המולקולרית. יתר על כן, המגוון הרחב של חומרים תואמים מאפשר ייצור לא רק של מבנים ממוזערים מסיליקון, כפי שמשמשים בשבבים, אלא גם של חומרים ביו-אקטיביים המתאימים לשילוב עם מערכות ביולוגיות. עם זאת, שיטות מעין אלו יקרות ולא מעשיות לייצור המוני של מוצרים ביו-רפואיים."
הצוות פיתח שיטות ננו-טכנולוגיות חסכוניות המתאימות לייצור הניתן להרחבה ברמה קלינית, וכבר ייצר אבות טיפוס ראשונים של משטחים מפעילים המסוגלים לייצר תאי CAR T בכמות המספיקה לטיפול בסרטן באדם מבוגר בקנה מידה קליני.
קבוצת המחקר כללה את הדוקטורנט עבד אל-קאדר יאסין, ובתר דוקטורנט ד"ר קרלוס אורנה מרטין, וכן חברים במספר קבוצות מחקר מאוניברסיטת בן-גוריון בנגב ומאוניברסיטת פנסילבניה.